全球首个!中国团队研究同时登上柳叶刀和 Nature 头条


独家抢先看
本文作者:ZJUN
中国学者的研究,再一次登上了 Nature 头条!
6 月 1 日,由北京大学沈琳教授团队设计主导的全球首个 CLDN18.2 CAR-T 胃癌随机对照研究的阳性结果正式发布于 the Lancet 上。
图源:参考资料 1
结果显示,在难治性实体瘤(晚期胃癌或胃食管结合部癌)中,该 CAR-T 细胞疗法相比标准疗法,显著延长了患者的中位无进展生存期和中位总生存期。这也是首次在实体瘤中取得良好疗效的 CAR-T 细胞疗法临床试验。[1]
今日,该研究结果也登上了 Nature 头条。
无进展生存期显著延长,总生存期延长 44%
CAR-T 细胞治疗的全称为:嵌合抗原受体 T 细胞免疫疗法。通过在实验室对收集的 T 细胞进行基因改造,使细胞生成嵌合抗原受体(CAR),这些 CAR 可以帮助 T 细胞识别癌细胞表面的抗原(或标记),并激活 T 细胞杀死这些癌细胞。
自 2017 年以来,美国 FDA 已经批准了 6 款 CAR-T 细胞疗法,用于治疗白血病、淋巴瘤等血液类恶性肿瘤。近年来,CAR-T 细胞疗法在系统性红斑狼疮、多发性硬化症等自身免疫病方面展现了巨大前景。
如今,关于 CAR-T 实体瘤的相关研究正如火如荼,但是,在胃肠道肿瘤方面,它的高证据等级研究还相对尚少。
本次主要研究的靶点是 Claudin18.2(CLDN18.2),它在多种恶性肿瘤(尤其是胃肠道肿瘤)中高表达,但在胃干细胞区不存在。因此,CLDN18.2 是一个理想的实体瘤治疗靶点。
而本次研究的疗法,Satricabtagene autoleucel(satri-cel)是一款靶向 CLDN18.2 的自体 CAR-T 细胞疗法(CLDN18.2-CAR-T),此前,沈琳、齐长松团队分别于 2022 年和 2024 年在 Nature Medicine 期刊发表了两篇论文。[2、3]
这两篇研究报道了 satri-cel 治疗实体瘤的 1 期临床数据,证明了该疗法在 CLDN18.2 表达阳性的晚期胃肠道肿瘤中显示出治疗潜力,且安全性可控。
图源:参考资料 3
而本次新发表的研究是延续此前研究的 2 期临床试验。该研究为中国开展的开放标签、多中心、随机对照临床试验,同时也是全球首个针对实体瘤的 CAR-T 细胞疗法随机对照临床试验。
该研究入组了 156 例 CLDN18.2 阳性(免疫组化染色强度 ≥2+ 且阳性肿瘤细胞 ≥40%)、至少接受过二线治疗但病情仍进展的晚期胃癌/胃食管结合部癌患者。
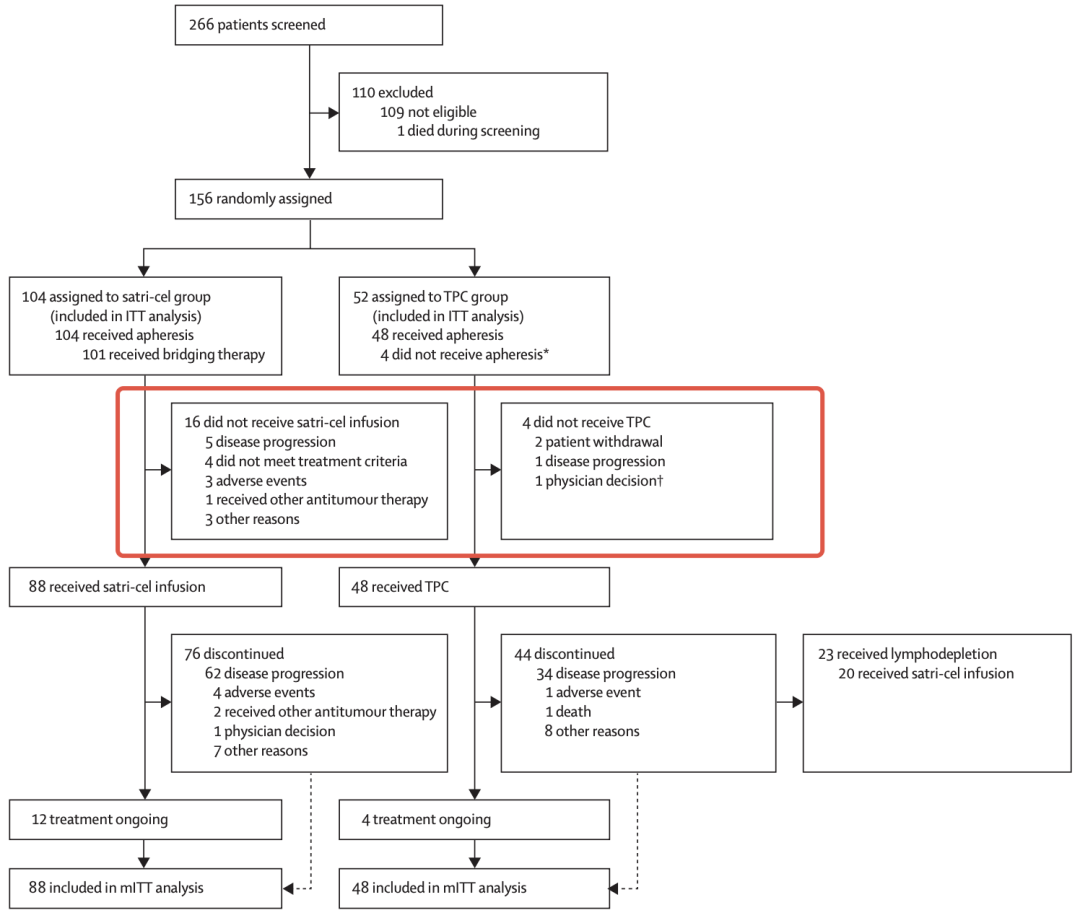
这些患者按照 2:1 随机分组,104 人被随机分配到 satri-cel 组,52 人被随机分配到医生选择治疗(TPC)组,其中 satri-cel 组输注自体 CAR-T 细胞,而 TPC 组则接受医生选择的包括纳武单抗、紫杉醇、多西他赛、伊立替康或阿帕替尼在内的标准治疗。
TPC 组有 20 人因为疾病进展或不能耐受,而接受了 satri-cel 治疗。最终,satri-cel 组有 88 人接受了治疗,TPC 组有 48 人接受了治疗。
图源:参考资料 1
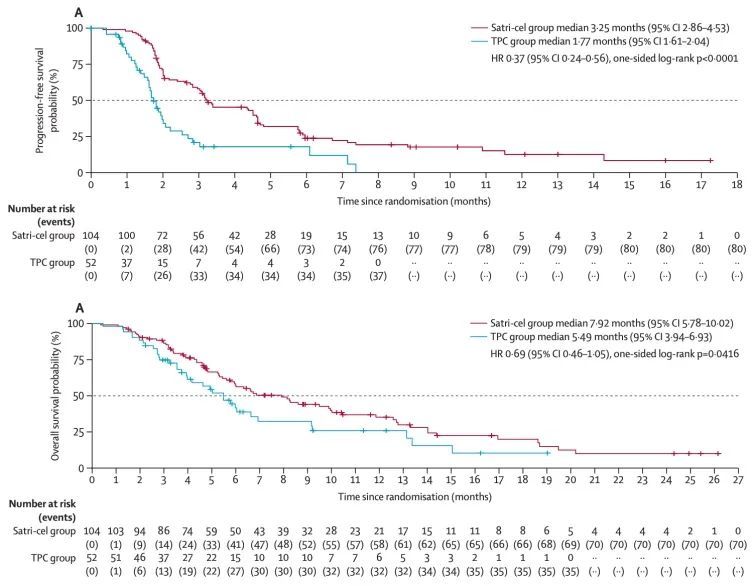
最终的研究结果显示,在有效性方面,satri-cel 组中位无进展生存期为 3.25 个月,TPC 组为 1.77 个月。satri-cel 组中位总生存期为 7.92 个月,TPC 组为 5.49 个月,相比标准疗法,satri-cel 将患者的中位总生存期延长了 44%。
无进展生存期与总生存期比较,图源:参考资料 1
此外,研究还揭示了 satri-cel 组客观缓解率(ORR)显著提高,已出现腹膜转移的患者(占全部患者的 66%)使用 satri-cel 治疗后,疾病进展风险显著降低。
安全性方面,satri-cel 组 99% 的患者发生了 ≥ 3级治疗相关不良事件,有 1 例患者死于治疗相关的弥散性血管内凝血。TPC 组的 ≥ 3级治疗相关不良事件发生率则为 63%。
这表示,接受 CAR-T 细胞治疗的患者的副作用发生率更高,该研究第一作者齐长松教授在接受 Nature 采访时表示,「CAR-T 细胞疗法的副作用更多,但许多副作用较为轻微。未来的试验将证明 CAR-T 细胞疗法能够使早期接受治疗的患者受益,而不是作为最后的治疗手段。」
图源:Nature 官网
CAR-T 治疗实体瘤的里程碑
目前,关于该研究的阳性结果,由齐长松教授在 2025 年美国临床肿瘤学会(ASCO)进行口头报告。
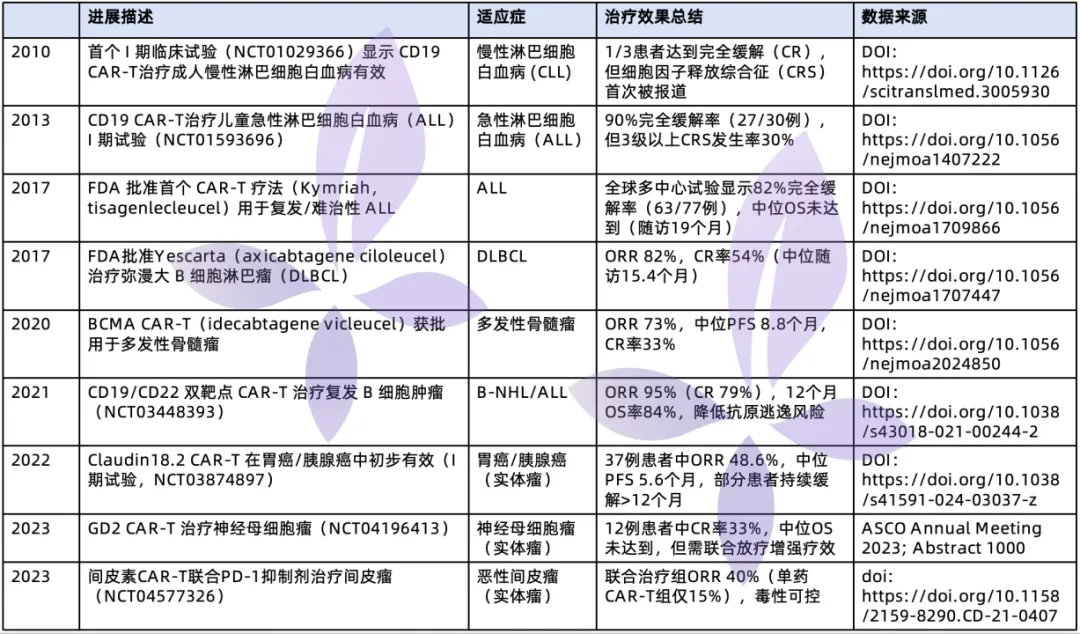
在该研究结果发布之前,丁香园曾对 2010 ~ 2023 年间,关于 CAR-T 细胞治疗的临床研究进行了不完全整理。
ORR:客观缓解率;CR:完全缓解;OS:总生存期;PFS:无进展生存期;CRS:细胞因子释放综合征。图源:丁香园整理
而此研究首次证明 CAR-T 细胞疗法在实体瘤中的疗效优于标准治疗。
研究团队在文章中指出:「据我们所知,这是全球首个在实体瘤中验证靶向 CLDN18.2 的 CAR-T 疗法疗效的随机对照试验。本研究首次提供了 CLDN18.2 作为胃癌和胃食管交界癌有效靶点的高级别临床证据。」这具有里程碑式的意义。
齐长松教授在 ASCO 2025 大会口头报告现场接受媒体采访时也表示,「这些结果表明,CLDN18.2 CAR-T 疗法可能带来晚期胃癌治疗的范式转变,为实体瘤治疗领域带来几乎前所未有的细胞治疗新选择。」[4]
但此研究也存在相应的局限性。
研究团队在文章中表示,首先,样本量以无进展生存期这一主要终点为准,因此亚组的分析结果可能不足以得出明确结论。其次,satri-cel 组有 16 例患者的 CAR-T 细胞在单采后无法输注,分析其原因,是因为肿瘤进展迅速,导致患者不再符合 CAR-T 细胞治疗的标准。
目前,对于肿瘤进展迅速的患者而言,单采和 CAR-T 细胞输注之间的时间间隔仍然是 CAR-T 细胞治疗的限制因素之一。研究团队还表示,未来随着 CAR-T 细胞技术的进步,这一问题有望得到解决。
策划:ZJUN | 监制:z_popeye
“特别声明:以上作品内容(包括在内的视频、图片或音频)为凤凰网旗下自媒体平台“大风号”用户上传并发布,本平台仅提供信息存储空间服务。
Notice: The content above (including the videos, pictures and audios if any) is uploaded and posted by the user of Dafeng Hao, which is a social media platform and merely provides information storage space services.”