辉瑞降压药再陷“召回门” 超标的致癌物到底来自哪儿?
作者|沙琼 陈家仪 陈安垚 编辑|沙琼
3月21日,辉瑞因为一起主动召回药品的通知,被曝光在聚光灯下——由于致癌杂质亚硝胺含量超标,辉瑞自愿召回3款常用降压药。
凤凰网健康发现,就在半个月前的3月4日,辉瑞加拿大公司在加拿大市场上全面召回同样的降血压药物。这两次召回的原因也相同。
凤凰网健康梳理发现近5年来,辉瑞在全美范围内共计召回14次,涉及16款药品,屡次深陷“召回门”,尽管是主动自愿召回,体现其积极担责的一面,但仍让这家历史近200年的全球药企不断遭遇药品质量安全的质疑。
药品本是治病的,为何辉瑞的救命药却可能带来致癌风险,到底问题出在哪儿?凤凰网健康带来独家解读——
辉瑞屡陷“召回门” 药物安全性遭质疑
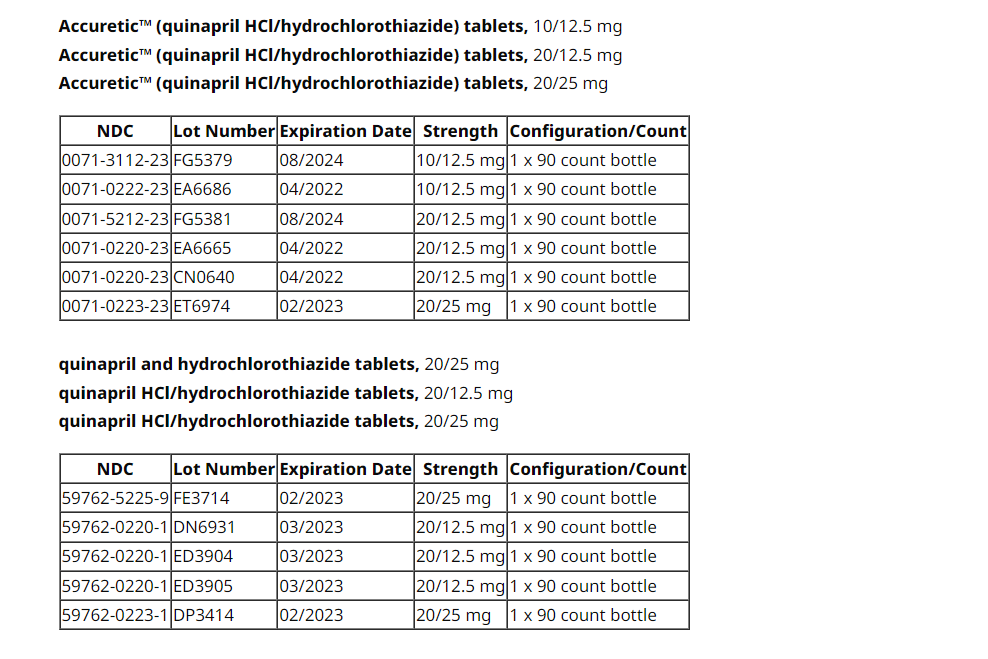
3月21日下午,辉瑞官网发布了一条召回通知:“由于存在亚硝胺,辉瑞公司自愿召回分销的Accuretic(盐酸喹那普利/氢氯噻嗪)片剂以及Greenstone分销的两种授权仿制药(喹那普利/氢氯噻嗪以及盐酸喹那普利/氢氯噻嗪)。因为药物中含有的N-亚硝基-喹那普利(亚硝胺杂质)高于人体每日可接受摄入量水平。辉瑞将召回6批次Accuretic片剂、1批次喹那普利和氢氯噻嗪片剂以及 4 批盐酸喹那普利/氢氯噻嗪片剂。”
辉瑞美国官网截图
辉瑞在其美国官网新闻稿中写到,“亚硝胺在水和食物中很常见,包括腌制和烤肉、乳制品和蔬菜。每个人都接触到一定程度的亚硝胺。如果人们长时间接触这些杂质超过可接受的水平,这些杂质可能会增加患癌症的风险。
这些产品适用于治疗高血压。降低血压可降低致命和非致命心血管事件的风险,主要是中风和心肌梗塞。这些产品的安全性已通过20多年的营销授权和强大的临床计划建立。迄今为止,辉瑞尚未收到经评估与此次召回相关的不良事件报告。”
辉瑞认为,根据目前可用的数据,产品的风险状况仍然是积极的。虽然长期摄入N-亚硝基-喹那普利可能与人类潜在的癌症风险增加有关,但服用这种药物的患者没有直接风险。目前服用这些产品的患者应咨询他们的医生以了解替代治疗方案。
辉瑞美国官网召回药品信息的截图
据其美国官网新闻中介绍,此次召回产品批次为2019年11月至2022年3月期间,分发给全美国和波多黎各的批发商和分销商。召回范围中没有提及是否涉及中国区域。
而就在半个月前的3月4日,辉瑞加拿大公司在加拿大市场上全面召回同样的降血压药物Accuretic片(盐酸喹那普利和氢氯噻嗪片)。Accurtic是一种处方药,含有盐酸喹那普利和氢氯噻嗪(quinapril hydrochloride and hydrochlorothiazide)的组合,这两种药物成分都可以降低血压。
此次召回原因同样是被查出含有潜在的致癌杂质亚硝胺含量超过了可接受的安全水平。长期暴露于较高水平可能会增加患癌的风险。
凤凰网健康详细梳理了一下,近5年来,辉瑞发布了14次在全美范围召回的通知,涉及16款药品,其中,涉及到亚硝胺超标而召回的有2款药品:
2022年3月1日因亚硝胺水平超限的原因,在加拿大宣布召回15批长效降压药Inderal-LA(盐酸普萘洛尔缓释胶囊);
2021年7月因N-亚硝基-伐尼克兰含量问题,辉瑞主动召回12批戒烟药物CHANTIX®(伐尼克兰)片剂。
在频繁的召回事件影响下,辉瑞的药品质量也不断受到质疑。
致癌物亚硝胺到底是什么?问题出在哪里?
为啥药物中屡次被发现致癌杂质亚硝胺?亚硝胺到底是什么?其超标的危害到底有多大?
凤凰网健康查询世界健康组织官网显示,亚硝胺,或更准确地说是N-亚硝基胺,是指任何含有亚硝基官能团的分子群。这些分子令人担忧,因为亚硝胺杂质可能是人类致癌物。虽然它们也存在于一些食物和饮用水供应中,但它们在药物中的存在仍然被认为是不可接受的。
2020年9月1日,美国食品药品监督管理局(简称FDA)颁布了《人用药中亚硝胺杂质控制》指南。已经确定了7种理论上可能存在于药品中的亚硝胺杂质:NDMA、N-亚硝基二甲胺(NDEA)、N-亚硝基-N-甲基-4-氨基丁酸(NMBA)、N-亚硝基异丙基乙胺(NIPEA)、N-亚硝基二异丙胺(NDPA)、N-亚硝二丁基胺(NDBA)和N-亚硝基甲基苯胺(NMPA)。其中五种(NDMA、NDEA、NMBA、NIPEA和NMPA)实际上已在API或药品中检测到。
当然,抛开剂量谈毒性是不严谨的,所以,世卫组织对于亚硝胺每日摄入量作了明确的限制:确定一种以上亚硝胺杂质,并且基于最大日剂量,亚硝胺杂质的总量超过26.5纳克/天(最强效亚硝胺的AI)。FDA认为,如果人们长时间接触亚硝胺杂质高于可接受的每日上限,则可能会增加患癌症的风险。
世界卫生组织对于亚硝胺每日摄入量限制的定义(世界卫生组织官网截图)
北京医院药学部副主任、主任药师金鹏飞向凤凰网健康介绍,此次辉瑞公司在美国召回的药品是盐酸喹那普利/氢氯噻嗪片,这是一个降血压的复方制剂,其中盐酸喹那普利属于临床使用广泛的血管紧张素转化酶抑制剂(ACEI)降压药,氢氯噻嗪是一种噻嗪类利尿,通过利尿而起到降压作用,临床上也很常用。这并不是第一次由于亚硝胺类杂质而对降压药进行召回。
早在2018年7月-2019年3月间,欧洲药品管理局(European Medicines Agency,EMA)和美国食品药品监督管理局(FDA)就陆续通报在缬沙坦、氯沙坦、厄贝沙坦等血管紧张素Ⅱ受体拮抗剂(ARB)降压药中检出N,N-二甲基亚硝胺(NDMA)、N,N-二乙基亚硝胺(NDEA)和N-亚硝基-N-甲基-4-氨基丁酸(NMBA)等亚硝酸类杂质,并对相关药品进行召回,引起了业内的广泛关注。
金鹏飞主任药师介绍,亚硝胺类杂质属于基因毒杂质,在低剂量时(μg甚至ng级)就可能引起DNA损伤,导致DNA突变,进而可能引发癌症和遗传毒性等严重后果;短时内大量摄入也可能直接导致死亡。
“其实,除了降压药,在二甲双胍、雷尼替丁、尼扎替丁、盐酸吡格列酮、利福平和利福喷丁等药物中也曾发现亚硝胺类杂质超标问题。”金鹏飞解释,为了加强对这类杂质的管理,2020年5月8日,国家药品监督管理局药品审评中心发布了《化学药物中亚硝胺类杂质研究技术指导原则(试行)》,旨在为注册申请上市以及已上市化学药品中亚硝胺类杂质的研究和控制提供指导,保证药品的安全和质量可控,实现有效的风险控制。”
为何致癌风险如此高的亚硝胺类杂质会经常出现在召回名单里?金鹏飞解释道,亚硝胺类杂质有多种产生原因,如工艺产生、降解途径和污染引入等。在药物合成中,胺类化合物与亚硝酸钠或其他亚硝化试剂反应可能产生亚硝胺类杂质;原料药生产过程中,使用了被亚硝胺类杂质污染的物料(起始物料、中间体、溶剂、试剂、催化剂等)也可能带来亚硝胺类杂质的风险;某些药物本身会降解产生亚硝胺类杂质,如雷尼替丁在高温下会产生亚硝胺类杂质。
若按照专家解读的观点,辉瑞的3款降压药出现亚硝胺杂质超标或许与药品原料及制作工艺相关。
那么,如何控制亚硝胺杂质的产生才是大家最关心的,金鹏飞解释,由于亚硝胺类杂质在人体中可接受限度较小,微量杂质的检测和控制难度大,因此对于亚硝胺类杂质的控制应采取避免为主、控制为辅的策略。对申报上市的产品,要求申请人在药品研发中应进行亚硝胺类杂质的风险评估;对于已上市药品,持有人或生产企业也应主动对于亚硝胺类杂质存在的风险进行评估,以防止或最小化患者亚硝胺类杂质的暴露。
降压药本是心血管患者的必备药,用来救命的,若因为亚硝胺杂质超标导致患癌风险增加,对于患者来说,救命药有可能会变成“致癌药”。
对于药企来说,药品关乎生命,安全是底线,尽管是辉瑞主动召回,但屡次深陷质量安全风波,都会对辉瑞的品牌形象带来不可修复的创伤。