国产创新药再传捷报:泽贝妥单抗III期临床研究结果在肿瘤免疫领域知名期刊正式发表
2024年10月3日,由博锐生物自主研发的国家1类创新药泽贝妥单抗(商品名:安瑞昔®)用于治疗CD20阳性弥漫大B细胞淋巴瘤的III期临床研究数据正式发表于美国癌症免疫治疗学会官方刊物《The Journal for ImmunoTherapy of Cancer》(IF:10.3)1。该研究结果已在2024年欧洲血液学协会年会(EHA 2024)上以壁报的形式公布。此次全文发表,体现了国际学术界对这一研究成果的再次认可,彰显了“中国创新药”的强劲实力。
行之有据,泽贝妥单抗可助力初治DLBCL患者实现更大获益
泽贝妥单抗和利妥昔单抗虽然均属于CD20单抗药物,但与利妥昔单抗相比,泽贝妥单抗通过差异化改造抗原结合表位和去岩藻糖使其具有更强的抗体依赖的细胞介导的细胞毒性(ADCC)作用、更大的表观分布容积和更持久的 B细胞清除作用。
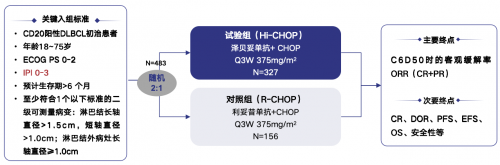
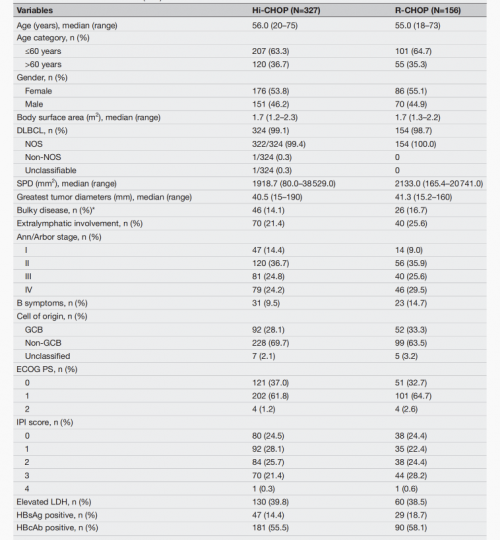
近期,一项多中心、随机、双盲III期临床研究证实了泽贝妥单抗联合CHOP(Hi-CHOP)方案(n=327)与R-CHOP(n=156)方案在初治CD20阳性DLBCL中的有效性和安全性。此研究的主要终点为C6D50时的客观缓解率(ORR),次要终点包括缓解持续时间(DOR)、无进展生存期(PFS)、无事件生存期(EFS)、总生存期(OS)、由盲法独立审查委员会(BIRC)评估的C6D50时的完全缓解率(CR)以及安全性(图1)1。此研究入组了伴大包块、结外受累、B症状等患者,两组患者的同质性相对较高,人口学特征和基线特征无显著差异(p>0.05)(表1)1。
图1.研究设计
表1. 患者基线特征
在全分析集(FAS)中,主要终点独立影像学委员会(IRC)评估的ORR在Hi-CHOP方案和R-CHOP方案中分别达到83.5%(95%CI:79.0%-87.3%)和81.4%(95%CI:74.4%-87.2%),组间差异为2.1%(95%CI:-5.2%-9.4%),Hi-CHOP方案的ORR相较于R-CHOP方案显示出更优的趋势;次要终点CR率Hi-CHOP方案也高于R-CHOP方案(75.2% vs 67.9%)(p=0.092)。
在符合方案集(PPS)中,Hi-CHOP方案和R-CHOP方案的ORR分别为95.3%(95%CI:92.2%-97.5%)和93.7%(95%CI:88.1%-97.3%),组间差异为1.6%(95%CI:3.3%至6.5%),PPS集中Hi-CHOP方案展现的ORR更优的趋势与FAS集相同;而在次要终点CR率方面,PPS分析显示Hi-CHOP方案比R-CHOP方案更优且具有统计学差异(85.7%vs 77.3%,p=0.038)。
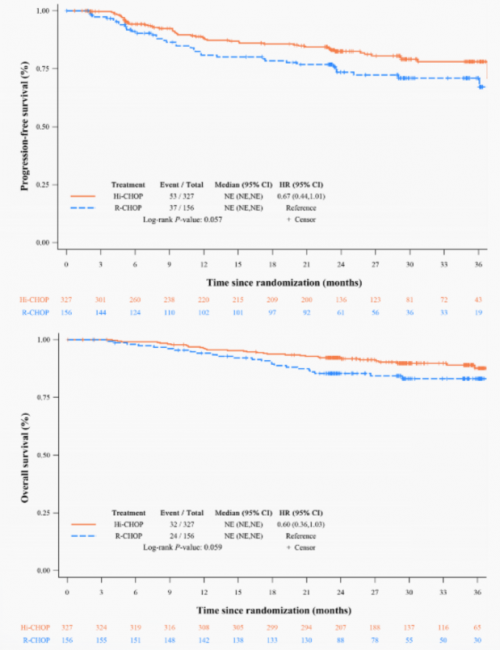
同时在全分析集(FAS)中,Hi-CHOP方案相较于R-CHOP方案的1-3年PFS率和1-3年OS率有更优的趋势(图2)。
图2. FAS集两组患者经BIRC评估的PFS和OS的Kaplan-Meier曲线
亚组分析显示,在FAS集中,对于GCB亚型的DLBCL患者,Hi-CHOP方案的ORR、CR率、EFS率及OS率均显著优于R-CHOP方案,同时Hi-CHOP方案的DOR(HR 0.47,95%CI:0.18-1.26;p=0.126)和PFS(HR 0.41,95%CI:0.16-1.07;p=0.060)也高于R-CHOP方案(表2)。而对于non-GCB亚型的DLBCL患者,Hi-CHOP方案和R-CHOP方案的DOR、PFS率、EFS率及OS率获益相当(P>0.05)。
安全性方面,Hi-CHOP方案与R-CHOP方案在治疗引起的不良事件(TEAE)(99.7% vs 100.0%,p=1.000)、药物相关TEAE(87.8% vs 82.1%,p=0.095)、严重不良事件(SAE)(44.3% vs 50.0%,p=0.283)和药物相关SAE(25.1%vs 27.6%,p=0.579)的发生率相似。
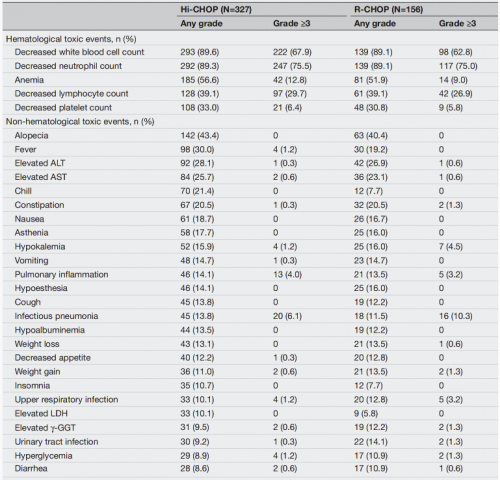
两组≥3级TEAE发生率分别为92.0%和92.3%,其中最常见的TEAE为中性粒细胞计数减少(75.5% vs 75.0%)、白细胞计数降低(67.9% vs 62.8%)、淋巴细胞计数减少(29.7% vs 26.9%)和贫血(12.8% vs 9.0%)(表2)。总体来说Hi-CHOP方案与R-CHOP方案的TEAE相似,安全性方面无显著差异。
表2. Hi-CHOP方案与R-CHOP方案的不良反应发生率(%)
该研究表明,泽贝妥单抗(375 mg/m2)联合CHOP在既往未经治疗的CD20阳性的中国DLBCL患者中,较经典R-CHOP方案表现出更高的完全缓解率且耐受性良好。。
泽贝妥单抗为CD20阳性DLBCL提供一线治疗新选择
弥漫大B细胞淋巴瘤(DLBCL)是非霍奇金淋巴瘤(NHL)中最常见的亚型,在我国约占35%~50%2。几十年来,R-CHOP方案一直是DLBCL的标准一线治疗方案,可治愈50%~70%患者,但仍有部分患者面临疾病难治或完全缓解后复发3。研究者们开展了大量研究以深入探索抗CD20单抗在DLBCL领域的疗效,结果均不尽人意4。
随着抗CD20单抗泽贝妥单抗的问世,DLBCL患者迎来了新的治疗曙光。临床前研究已经显示,泽贝妥单抗的抗体依赖性细胞介导的细胞毒作用(ADCC)以及药代动力学和药效学均优于利妥昔单抗。此次III次临床研究更是向全球展示了泽贝妥单抗在CD20 DLBCL患者中的疗效优势,且耐受性良好1。
博锐生物CEO王海彬博士表示:“长久以来,如何突破R-CHOP方案的治疗瓶颈,实现疗效的新飞跃,一直是我们面临的重要挑战。泽贝妥单抗的问世,为我们提供了解决这一难题的关键答案。我们很高兴看到泽贝妥单抗在治疗CD20阳性弥漫大B细胞淋巴瘤患者中展示出的良好的抗肿瘤活性和可控的安全性,凸显了其在相关适应症等领域的巨大治疗潜力和重要临床价值。目前,泽贝妥单抗已获得《中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南(2023版)》和《淋巴瘤免疫治疗中国专家共识(2024年版)》权威推荐5,6,并在《中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南(2024版)》中持续进行了推荐7,同时成功取得中国澳门特别行政区政府药物监督管理局(ISAF)的上市许可8,展望未来,我们将持续推进临床项目,致力于为全球患者提供更多元化、更有效的治疗选择。”
关于安瑞昔®(泽贝妥单抗)
安瑞昔®(泽贝妥单抗)是一种新型抗CD20单抗,是我国自主研发的1类创新型生物制品,获重大新药创制科技重大专项资助。研究数据显示,与利妥昔单抗相比,泽贝妥单抗通过差异化改造抗原结合表位和去岩藻糖使得安瑞昔®具有更强的ADCC作用,更大的表观分布容积和更持久的B细胞清除作用。
关于弥漫大B细胞淋巴瘤
弥漫性大B细胞淋巴瘤(DLBCL)是一种来源于成熟B细胞的侵袭性肿瘤,是最常见的非霍奇金淋巴瘤类型,约占全部非霍奇金淋巴瘤的25%~50%。DLBCL异质性大,常累及淋巴结及淋巴系统外的器官或组织。
参考文献:
1.Li Z, Jiang W, Zhou H, et al. Comparison of zuberitamab plus CHOP versus rituximab plus CHOP for the treatment of drug-naïve patients diagnosed with CD20-positive diffuse large B-cell lymphoma: a phase 3 trial. J Immunother Cancer. 2024;12(10):e008895.
2.国家卫生健康委. 淋巴瘤诊疗指南(2022年版).
Munoz J, Deshpande A, Rimsza L, Nowakowski GS, Kurzrock R. Navigating between Scylla and Charybdis: A roadmap to do better than Pola-RCHP in DLBCL. Cancer Treat Rev. 2024;124:102691.
Sehn LH, Martelli M, Trněný M, et al. A randomized, open-label, Phase III study of obinutuzumab or rituximab plus CHOP in patients with previously untreated diffuse large B-Cell lymphoma: final analysis of GOYA. J Hematol Oncol. 2020;13(1):71.
中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南(2023年版). [M].人民卫生出版社, 2023.4.
淋巴瘤免疫治疗中国专家共识(2024年版)[J].肿瘤综合治疗电子杂志,2024,10(02):69-98.
中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南(202年版). [M].人民卫生出版社, 2023.4.
https://www.isaf.gov.mo.