2025 ASCO:中外大咖巅峰访谈,共同探讨 ADC 治疗晚期 NSCLC 新进展


独家抢先看
盛夏将至,骄阳似火。近日,2025 年美国临床肿瘤学会(ASCO)圆满落幕。作为全球肿瘤学领域规模最大、最具影响力的学术盛会之一,本届年会汇聚全球肿瘤领域权威专家,共同探讨癌症治疗的最新突破与临床实践创新。
其中,抗体药物偶联物(ADC)是近年来恶性肿瘤领域的研究热点,已悄然间改变包含非小细胞肺癌(NSCLC)在内的诸多实体瘤的治疗格局。为进一步交流国内外 ADC 在肺癌领域的突破性进展,共同促进肿瘤医学专业信息的传递及医学知识的传播,从而推动我国临床肿瘤事业的发展。丁香园联合美中抗癌协会(USCACA)特别邀请中山大学肿瘤防治中心张力教授、IASLC 首席科学官(CSO)Prof. Jennifer King 教授,基于中美两国专家视角,共同探讨 ADC 在晚期 NSCLC 中的应用的若干问题。
视频 1:张力教授访谈视频
视频 2:Prof. Jennifer King 访谈视频
捷报频传:ADC 进展迅速,诸多研究闪耀 2025 ASCO
张力教授介绍,ADC 是肺癌领域的热点,2025 ASCO 大会共计收录 60 余项 ADC 领域研究,诸多研究值得关注。其中 TROP2 ADC —— 芦康沙妥珠单抗有多项临床研究在此次 ASCO 会议中亮相,包括 OptiTROP-Lung01 研究、OptiTROP-Lung03 研究、SKB264-II-08 研究等。从驱动基因阴性到 EGFR 突变,从后线到一线,这些研究覆盖了广泛人群,为肺癌患者提供了治疗新希望。此外,双特异性 ADC iza-bren 用于 NSCLC 和 小细胞肺癌(SCLC)的两项 I 期临床研究也十分值得关注。
Jennifer King 教授则表示,本次 ASCO 大会中,诸多研究聚焦于 EGFR-TKI 耐药后的治疗探索,其中芦康沙妥珠单抗用于既往接受过治疗的晚期 EGFR 突变 NSCLC 的 OptiTROP-Lung03 研究结果十分值得关注,充分证实了芦康沙妥珠单抗在这部分患者中的疗效及安全性[1]。
关于 ADC 对肺癌治疗格局的影响,张力教授指出,ADC 目前已在 NSCLC 后线治疗中占据「一席之地」,有望重塑肺癌治疗格局。其中众多研究数据显示了 TROP2 ADC 在晚期经治 NSCLC 中的疗效,芦康沙妥珠单抗是肺癌领域首个获批适应症的 TROP2 ADC,已成为既往经治 EGFR 突变晚期 NSCLC 患者新的治疗标准;此外,靶向 HER2 的 ADC 也已获批相关后线适应症。而随着研究的深入,ADC 针对晚期 NSCLC 的治疗策略正逐步由后线向一线探索扩展。如在驱动基因阴性患者中,II 期 OptiTROP-Lung01 研究探索了芦康沙妥珠单抗联合 PD-L1 抑制剂塔戈利单抗一线治疗的疗效;在 EGFR 阳性 NSCLC 患者中,SKB264-III-15 研究将探索芦康沙妥珠单抗联合奥希替尼一线治疗的疗效。
当然,ADC 在肺癌领域的探索并非一帆风顺,此次会议中 HER3-DXd 对比培美曲塞/卡铂用于治疗既往接受过 EGFR-TKI 治疗失败的局部晚期或转移性 EGFR 突变 NSCLC 的 HERTHENA-Lung02 研究结果公布,总生存期 OS 未达到统计学意义[2]。张力教授表示,这进一步提示我们,针对不同的 ADC 药物,需进行获益人群的筛选。
重塑新生:芦康沙妥珠单抗闪耀 ASCO 舞台,展现肺癌治疗「硬实力」
值得关注的是,张力教授团队共有 2 项芦康沙妥珠单抗相关研究入围本次 ASCO 大会,分别聚焦于经治 EGFR 突变耐药人群及 EGFR 罕见突变人群。张力教授介绍,前期基础及转化研究结果显示,EGFR 突变可通过增强 TROP2 ADC 的内吞作用提升药物抗肿瘤活性,解释了其在 EGFR 突变型和野生型患者中的疗效差异[3]。基于此,其所在团队开展了 OptiTROP-Lung03 研究,入组患者以 2:1 的比例随机分组接受芦康沙妥珠单抗或多西他赛治疗。
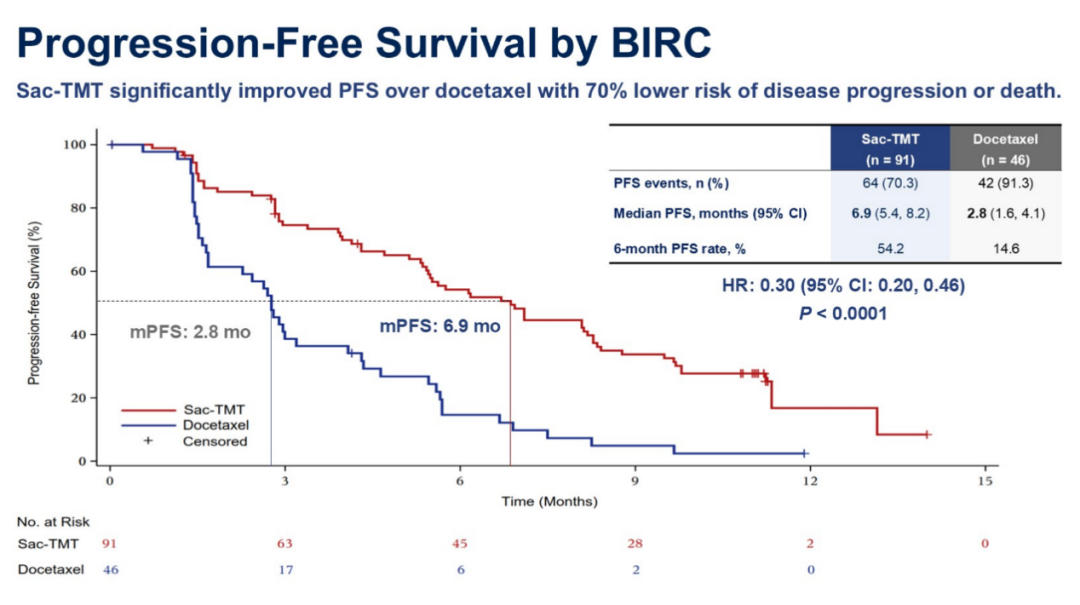
结果显示,与多西他赛相比,芦康沙妥珠单抗在疗效方面取得了显著统计学意义和临床意义的成果:芦康沙妥珠单抗组经 BIRC 评估的客观缓解率(ORR)相比多西他组提升近 3 倍(45.1% vs 15.6%;单侧 P = 0.0004);BIRC 评估的中位无进展生存期(mPFS)延长了 4.1 个月(6.9 个月 vs 2.8 个月;HR = 0.30, 单侧 P < 0.0001),显著降低疾病进展或死亡风险 70%。
图 1:BICR 评估的确认 ORR
图 2:BICR 评估的 PFS
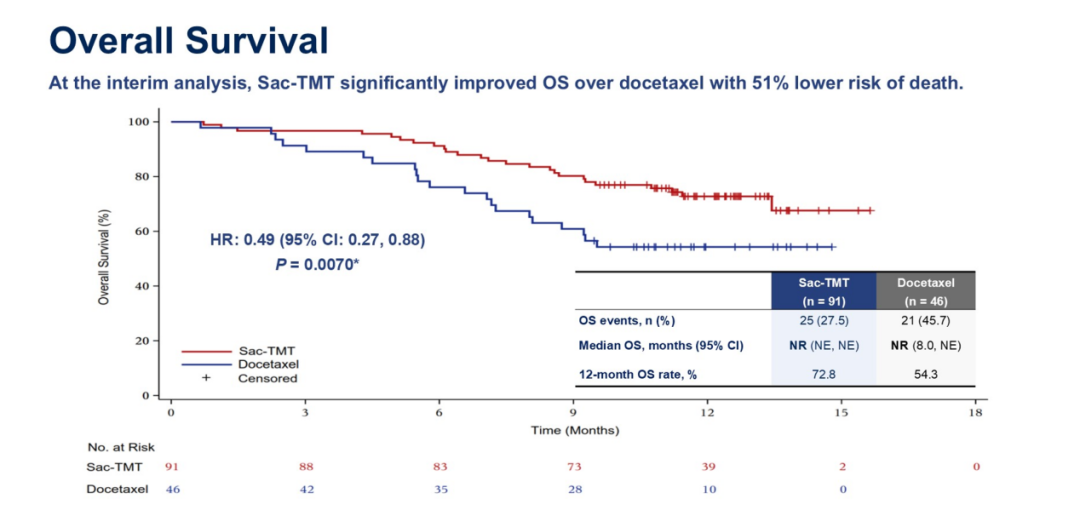
两组的中位 OS 均尚未达到,但中期分析结果显示,相较于多西他赛,芦康沙妥珠单抗能够降低疾病死亡风险 51%(HR = 0.49,单侧 P =0.007)[1]。由于多西他赛组中有 36.4% 的患者交叉接受了芦康沙妥珠单抗治疗,经 RPSFT 模型校正交叉治疗对 OS 的影响,芦康沙妥珠单抗相较多西他赛降低死亡风险 64%(HR = 0.36)。该研究结果促使芦康沙妥珠单抗在中国获批用于治疗经 EGFR-TKI 和含铂化疗后进展的 EGFR 突变阳性局部晚期或转移性非鳞状 NSCLC,并标志着其成为全球第一个获批用于肺癌的 TROP2 ADC。
图 3:OS 曲线
另一项研究则为芦康沙妥珠单抗用于经治罕见 EGFR 突变晚期 NSCLC 患者的 II 期临床研究(SKB264-II-08 第一部分队列 5),该研究入选本次大会壁报展示环节,是首个报道 TROP2 ADC 用于经治 EGFR 罕见突变 NSCLC 疗效和安全性的临床研究。截至 2024 年 12 月 1 日,共入组 42 例患者,包括 23 例 L861Q、S768I、G719X 等患者(队列 a),19 例 ex20ins 患者(队列 b)。整体人群的 ORR 为 35.7%,疾病控制率(DCR)为 85.7%,mPFS 达 9.5 个月。亚组分析显示,非 ex20ins 突变亚组的 ORR 为 34.8%,mPFS 为 10.9 个月;ex20ins 突变亚组 ORR 为 36.8%,mPFS 为 9.0 个月[4]。该研究数据为经治 EGFR 罕见突变患者带来了治疗新希望。
表 1:研究者评估的疗效
图 4:PFS 曲线
不仅仅在驱动基因阳性人群中的疗效表现亮眼,在驱动基因阴性人群的治疗中芦康沙妥珠单抗同样交出了令人振奋的答卷。张力教授指出,长久以来免疫联合化疗是驱动基因阴性人群的一线标准治疗,然而 PFS 多维持在 7-11 个月,如何优化这部分患者的治疗预后是临床上亟待解决的难题。
在此种背景下,OptiTROP-Lung01 研究探索了芦康沙妥珠单抗联合 PD-L1 抑制剂塔戈利单抗用于驱动基因阴性晚期 NSCLC 一线治疗的疗效和安全性。2024 年 ASCO 会议中首次公布的研究结果证实,芦康沙妥珠单抗 5 mg/kg Q2W + 塔戈利单抗 900 mg Q2W 治疗的 ORR 达 69%,DCR 为 100%,mPFS 尚未达到[5]。此次 ASCO 公布的非鳞亚组结果进一步夯实了该联合治疗方案的治疗获益,研究结果证实芦康沙妥珠单抗联合塔戈利单抗一线治疗驱动基因阴性非鳞癌患者的 ORR (59.3%)和 mPFS(15.0 个月) 均超越现有标准治疗;尤其在 PD-L1 表达阴性人群中,mPFS 突破 1 年[6]。
表 2:非鳞队列疗效结果
图 5:不同PD-L1 表达水平亚组的 PFS 曲线
6 月 3 日,CDE 官网显示,芦康沙妥珠单抗联合塔戈利单抗一线治疗驱动基因阴性局部晚期或转移性非鳞状 NSCLC 拟纳入突破性疗法认定。期待该适应症的获批,重新定义晚期非鳞 NSCLC 一线治疗格局,为我国肺癌患者提供更高效的治疗选择。
无限前景:ADC 在肺癌领域大有可为,中外协作将带来更多可能
张力教授认为,尽管当前 ADC 用于晚期 NSCLC 的治疗已取得诸多突破性进展,但仍有诸多悬而未决的问题值得进一步探索。首先,并非所有患者均可从 ADC 中获益,通过生物标志物等精准筛选更能实现治疗获益的人群至关重要。其次,提升 ADC 药物的疗效是临床探索的重要方向,未来可进一步开发新靶点 ADC 和探索全新的联合治疗方案,确定最具潜力的联合策略(如 ADC + 免疫、ADC + 靶向等),优化给药方案和治疗顺序。与此同时,明确 ADC 药物的耐药机制同样是未来研究的重点之一。例如,肿瘤细胞可能通过减少表面抗原表达、不释放药物或将药物泵出细胞等方式产生耐药性。针对这些机制,制定相应的对策将有助于延缓耐药性的发生。此外,不良反应的管理同样值得关注,ADC 药物的不良反应主要分为与靶点相关和与载荷相关的不良反应,如何平衡好 ADC 药物疗效和安全性的关系,也是大家未来亟需解决的问题。
作为 IASLC 首席科学馆,Jennifer King 教授表示,IASLC 致力于推进肺癌临床研究的全球化,并付出了诸多努力,譬如制定并推广全球范围内的统一肺癌分期系统等。考虑到不同种族、不同地区患者存在不同的生物学特点,因此在临床研究中对不同代表性的患者进行分层并深入分析十分重要,这有助于帮助研究者了解药物在不同类型患者中的疗效和潜能,进而为全球性研究提供参考。令人欣慰的是,目前肺癌领域的诸多研究都是全球性研究,其中也包含很多跨国性研究,推动了全球制药领域的快速、高质量发展。得益于全球性研究的开展,目前有诸多中国药物在美国上市,为美国患者带来更多获益。未来期待中美继续加深合作,合力创新书写肿瘤患者更加美好的未来。
小结
2025 ASCO 年会充分展示了 ADC 在晚期 NSCLC 治疗中的巨大潜力。其中,芦康沙妥珠单抗有多项研究在此次会议中亮相,其在经治 EGFR 经典和罕见突变中疗效显著,并在驱动基因阴性患者一线联合治疗中展现出超越现有标准疗法的研究成果。
在取得优异成绩的同时,我们还需认识到目前 ADC 的应用仍存在挑战(如人群筛选、耐药、安全性管理等),相信未来通过精准医疗、新药/联合方案研发及全球合作等,ADC 有望进一步重塑肺癌治疗格局,为更多患者带来更优的治疗选择。
内容审核:方程
项目审核:于轩
参考文献
[1]Li Zhang, Wenfeng Fang, Xingya Li, et al. Sacituzumab tirumotecan (sac-TMT) in patients (pts) with previously treated advanced EGFR-mutated non-small cell lung cancer (NSCLC): Results from the randomized OptiTROP-Lung03 study. 2025 ASCO Abstract 8507.
[2]Tony Mork, et al. Patritumab deruxtecan (HER3-DXd) in resistant EGFR-mutated (EGFRmadvanced non-small cell lung cancer (NSCLC) after a third-generationEGFR TKl: The phase 3 HERTHENA-Lung02 study. 2025 ASCO. Abstract 8506.
[3]Zhao S, et al. Sacituzumab tirumotecan in advanced non-small-cell lung cancer with or without EGFR mutations: phase 1/2 and phase 2 trials[J]. Nat Med. 2025 Apr 10. doi: 10.1038/s41591-025-03638-2.
[4]Li Z, et al. Sacituzumab tirumotecan (sac-TMT) in patients (pts) with previously treated locally advanced or metastatic (LA/M) non-small cell lung cancer (NSCLC) harboring uncommon EGFR mutations: Preliminary results from a phase 2 study. ASCO 2025, Abstract 861.
[5]Fang W, et al. Sacituzumab Tirumotecan (Also Known as SKB264/MK-2870) in Combination With KL-A167 (Anti‒PD-L1) as First-Line Treatment for Patients With Advanced NSCLC From the Phase II OptiTROP-Lung01 Study. ASCO 2024. Abstract 8502.
[6]Fang W, et al. Sacituzumab tirumotecan (sac-TMT) in combination with tagitanlimab (anti-PD-L1) in first-line (1L) advanced non-small-cell lung cancer (NSCLC): Non-squamous cohort from the phase II OptiTROP-Lung01 study. ASCO 2025. Abstract 8529.
“特别声明:以上作品内容(包括在内的视频、图片或音频)为凤凰网旗下自媒体平台“大风号”用户上传并发布,本平台仅提供信息存储空间服务。
Notice: The content above (including the videos, pictures and audios if any) is uploaded and posted by the user of Dafeng Hao, which is a social media platform and merely provides information storage space services.”